Μελέτες δείχνουν ότι ένζυμα χρησιμοποιούν κβαντική σήραγγα για να μεταφέρουν υδρογόνο στοιχεία. Χωρίς κβαντικά φαινόμενα, η βιολογική κατάλυση θα ήταν πολύ αργή για τη ζωή.
⚗️ Ένζυμα — οι αόρατοι επιταχυντές της ζωής
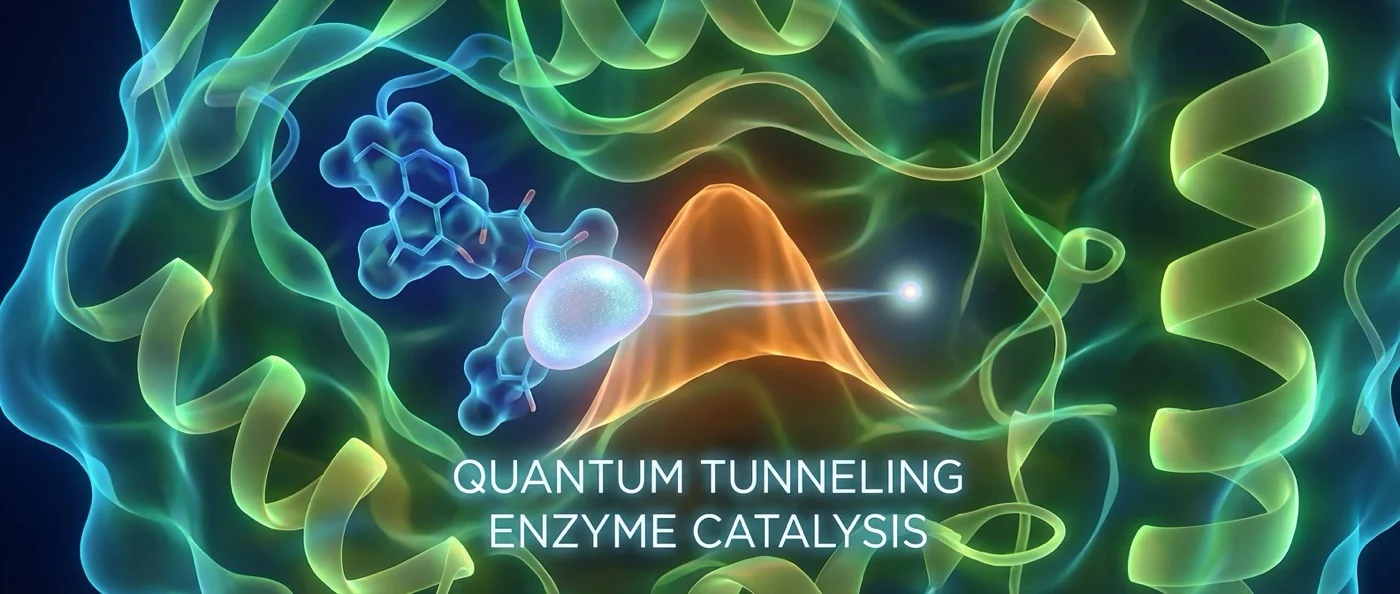
Κάθε δευτερόλεπτο, δισεκατομμύρια χημικές αντιδράσεις συμβαίνουν μέσα στα κύτταρά μας. Η πέψη, η αναπνοή, η σύνθεση DNA — τίποτα δεν θα ήταν δυνατό χωρίς τα ένζυμα, τις πρωτεΐνες που επιταχύνουν τις βιολογικές αντιδράσεις κατά εκατομμύρια φορές. Στην κλασική βιοχημεία, τα ένζυμα δρουν μειώνοντας το λεγόμενο «φράγμα ενεργοποίησης» — την ελάχιστη ενέργεια που χρειάζεται μια αντίδραση για να ξεκινήσει. Αλλά υπάρχει ένα μυστήριο: ορισμένα ένζυμα λειτουργούν ταχύτερα από ό,τι προβλέπει η κλασική θεωρία. Η εξήγηση βρίσκεται στην κβαντική μηχανική.
🔀 Κβαντική σήραγγα — η συντόμευση μέσα από το αδύνατο
Στον κλασικό κόσμο, αν μια μπάλα δεν έχει αρκετή ενέργεια να περάσει πάνω από έναν τοίχο, σταματάει. Στον κβαντικό κόσμο, τα πράγματα είναι διαφορετικά. Τα σωματίδια — πρωτόνια, ηλεκτρόνια, ιόντα υδρογόνου — συμπεριφέρονται ταυτόχρονα σαν κύματα. Αυτή η κυματική φύση τους επιτρέπει να «περάσουν μέσα» από ενεργειακά φράγματα που κλασικά θα ήταν αδιαπέραστα. Το φαινόμενο ονομάζεται κβαντική σήραγγα (quantum tunneling).
Στα ένζυμα, αυτό συμβαίνει σε αποστάσεις της τάξης του 1 Ångström (10⁻¹⁰ μέτρα) — περίπου όσο ένας χημικός δεσμός. Τα ιόντα υδρογόνου (H⁺) και τα ηλεκτρόνια δεν χρειάζεται να «σκαρφαλώσουν» πάνω από το ενεργειακό φράγμα. Μπορούν να το διαπεράσουν κβαντικά — σαν να περνούν μέσα από τον τοίχο αντί να πηδούν πάνω του.
🔬 Η ανακάλυψη — πρώτα ενδεικτικά στοιχεία
Η ιστορία ξεκίνησε το 1966, σε ένα εργαστήριο που μελετούσε φωτοσυνθετικά βακτήρια. Οι Don DeVault και Britton Chase μελέτησαν το βακτήριο Chromatium και παρατήρησαν κάτι αξιοσημείωτο: σε θερμοκρασίες κάτω από 100 K (−173 °C), ο ρυθμός οξείδωσης του κυτοχρώματος δεν μειωνόταν — ήταν ανεξάρτητος θερμοκρασίας. Κλασικά, χαμηλότερη θερμοκρασία σημαίνει λιγότερη κινητική ενέργεια και πιο αργές αντιδράσεις. Η εξήγηση; Τα ηλεκτρόνια δεν περνούσαν «πάνω» από το φράγμα — πέρναγαν «μέσα» μέσω κβαντικής σήραγγας.
Τρεις δεκαετίες αργότερα, η Judith Klinman στο Πανεπιστήμιο Berkeley έφερε την κρίσιμη απόδειξη. Το 1994, μελέτη στη λιποξυγενάση σόγιας (soybean lipoxygenase) αποκάλυψε «εξαιρετικά μεγάλα κινητικά ισοτοπικά αποτελέσματα» (kinetic isotope effects, KIE). Όταν το κανονικό υδρογόνο αντικαθίσταται από δευτέριο — ένα βαρύτερο ισότοπο — η αντίδραση επιβραδύνεται. Κλασικά, η επιβράδυνση πρέπει να είναι μέτρια (KIE ≈ 7). Στη λιποξυγενάση όμως, η επιβράδυνση ήταν 80 φορές μεγαλύτερη — πολύ πέρα από κάθε κλασική πρόβλεψη. Αυτό ήταν σαφές αποτύπωμα κβαντικής σήραγγας.
⚛️ Masgrau 2006 — η ατομική περιγραφή
Η πληρέστερη επιβεβαίωση ήρθε τον Απρίλιο του 2006, σε δημοσίευση στο κορυφαίο περιοδικό Science. Η ομάδα της Laura Masgrau, μαζί με τους Roujeinikova, Johannissen και συνεργάτες, κατάφεραν κάτι πρωτόγνωρο: περιέγραψαν σε ατομικό επίπεδο μια ενζυμική αντίδραση που κυριαρχείται πλήρως από σήραγγα πρωτονίων.
Το ένζυμο ήταν η αρωματική αμινοαφυδρογονάση (aromatic amine dehydrogenase, AADH) κατά την οξείδωση τρυπταμίνης. Με συνδυασμό κρυσταλλογραφίας ακτίνων Χ, κινητικών μετρήσεων και υπολογιστικών προσομοιώσεων, η ομάδα έδειξε ότι η μεταφορά πρωτονίου δεν ακολουθεί την κλασική θεωρία μεταβατικής κατάστασης. Η σήραγγα δεν ήταν μικρή διόρθωση — ήταν ο κυρίαρχος μηχανισμός της αντίδρασης.
Γιατί είναι σημαντικό: Η μελέτη Masgrau et al. (2006) στο Science έδειξε ότι η κβαντική σήραγγα πρωτονίων μπορεί να είναι ο κυρίαρχος μηχανισμός αντίδρασης σε ορισμένα ένζυμα — όχι μια μικρή κβαντική διόρθωση, αλλά η βάση ολόκληρης της κατάλυσης.
Η αρχή αυτή ισχύει ευρέως. Η ανασκόπηση των Nagel και Klinman (2006) στο Chemical Reviews κατέληξε στο συμπέρασμα ότι η κβαντική σήραγγα παίζει σημαντικό ρόλο στη μεταφορά υδριδίων (hydride transfer) σε πολλά ένζυμα ζωικών οργανισμών.
⚡ Μιτοχόνδρια — η κβαντική μηχανή ενέργειας
Αν τα ένζυμα είναι οι εργάτες του κυττάρου, τα μιτοχόνδρια είναι οι σταθμοί ηλεκτροπαραγωγής. Η αλυσίδα μεταφοράς ηλεκτρονίων (electron transport chain, ETC) μετατρέπει τη βιομάζα τροφής σε ATP — το ενεργειακό νόμισμα της ζωής. Και σε αυτή τη διαδικασία, η κβαντική σήραγγα είναι βασικός πρωταγωνιστής.
Η εσωτερική μεμβράνη των μιτοχονδρίων έχει πάχος μόλις ~7,5 nm. Μέσα σε αυτήν, τα ηλεκτρόνια διεισδύουν μέσω κβαντικής σήραγγας στα σύμπλοκα I (NADH:ουβικινόνη οξειδοαναγωγάση) και III (CoQH₂-κυτόχρωμα c αναγωγάση). Η θερμοδυναμική αποδοτικότητα αυτής της μετατροπής αγγίζει το 60-70% — πολύ ανώτερη από οποιαδήποτε μηχανή κατασκευασμένη από τον άνθρωπο.
Η φερριτίνη — μια πρωτεΐνη αποθήκευσης σιδήρου που βρίσκεται σε φυτά και ζώα — εμφανίζει κβαντική σήραγγα ηλεκτρονίων σε αποστάσεις μέχρι 8 nm σε θερμοκρασία δωματίου. Η σήραγγα αυτή είναι ανεξάρτητη θερμοκρασίας — ακριβώς όπως πρώτος υπέθεσε ο DeVault το 1966 — υποδηλώνοντας ότι είναι ουσιαστικά συμφωνική (coherent). Ένα αξιοσημείωτο κβαντικό φαινόμενο σε θερμό, θορυβώδες βιολογικό περιβάλλον.
🧬 Οι ευρύτερες επιπτώσεις — κβαντική βιολογία
Η κβαντική σήραγγα στα ένζυμα δεν είναι ακαδημαϊκή περιέργεια — είναι πιθανώς κρίσιμη για την ύπαρξη της ζωής. Χωρίς τη σήραγγα, ο ρυθμός πολλών ενζυμικών αντιδράσεων θα ήταν ~1000 φορές πιο αργός. Αρκετά αργός ώστε η βιολογική κατάλυση να μην μπορεί να στηρίξει τον μεταβολισμό.
«Η κβαντική βιολογία θέτει ένα συναρπαστικό ερώτημα: εκμεταλλεύεται η ζωή κβαντικά φαινόμενα με μη τετριμμένους τρόπους;» — Jim Al-Khalili, φυσικός, TED Talk 2015
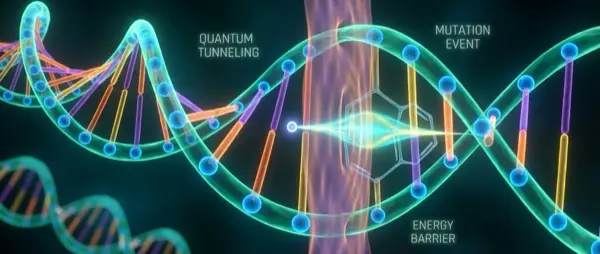
Πέρα από τα ένζυμα, η κβαντική σήραγγα εμπλέκεται και σε μεταλλάξεις DNA. Η μεταφορά πρωτονίων μεταξύ βάσεων μπορεί να προκαλέσει ταυτομερή μετατόπιση — αλλαγή στη δομή ενός νουκλεοτιδίου που οδηγεί σε λανθασμένη αντιγραφή. Μελέτη των Slocombe, Al-Khalili και Sacchi (2021) στο Physical Chemistry Chemical Physics έδειξε ότι η κβαντική σήραγγα πρωτονίων μπορεί να προκαλεί σημειακές μεταλλάξεις στα ζεύγη βάσεων AT και GC. Η κβαντική μηχανική δεν τροφοδοτεί μόνο τη ζωή — μπορεί να οδηγεί και τις μεταλλάξεις επί των οποίων δρα η φυσική επιλογή.
Σήμερα, ο τομέας της κβαντικής βιολογίας εξελίσσεται ραγδαία. Ερευνητές μελετούν πώς η κατανόηση της σήραγγας μπορεί να βοηθήσει στη σχεδίαση νέων φαρμάκων — αν γνωρίζουμε ακριβώς πώς ένα ένζυμο χρησιμοποιεί κβαντική σήραγγα, μπορούμε να σχεδιάσουμε αναστολείς που στοχεύουν αυτόν τον μηχανισμό. Η κβαντική χημεία υπολογιστών ανοίγει νέα πεδία σε αυτή την κατεύθυνση.
Από τα φωτοσυνθετικά βακτήρια που μελέτησε ο DeVault μέχρι τα μιτοχόνδρια κάθε κυττάρου μας, η κβαντική σήραγγα βρίσκεται στην καρδιά της βιολογικής κατάλυσης. Τα ένζυμά μας δεν λειτουργούν «παρά» τη φυσική — λειτουργούν μέσα σε αυτή, εκμεταλλευόμενα τις πιο παράδοξες ιδιότητες του κβαντικού κόσμου.