Το μοντέλο Μπορ εξηγεί τη σταθερότητα του ατόμου εισάγοντας κβαντισμένες τροχιές ηλεκτρονίων. Πώς ο Νιλς Μπορ ενσωμάτωσε κβαντικές ιδέες στο ατομικό πρότυπο.
📖 Διαβάστε περισσότερα: Κατάρρευση κυματοσυνάρτησης: Το μυστήριο της παρατήρησης
⚛️ Το Πρόβλημα του Κλασικού Ατόμου
Στις αρχές του 20ού αιώνα, ο Ernest Rutherford πρότεινε ένα μοντέλο ατόμου όπου τα ηλεκτρόνια περιστρέφονται γύρω από έναν θετικά φορτισμένο πυρήνα — κάτι σαν ένα μικροσκοπικό ηλιακό σύστημα. Η εικόνα ήταν κομψή, αλλά έκρυβε ένα θανάσιμο πρόβλημα: σύμφωνα με την κλασική ηλεκτρομαγνητική θεωρία του Maxwell, κάθε φορτισμένο σωματίδιο που επιταχύνεται εκπέμπει ηλεκτρομαγνητική ακτινοβολία.
Ένα ηλεκτρόνιο σε κυκλική τροχιά βρίσκεται σε συνεχή επιτάχυνση (κεντρομόλος). Αυτό σημαίνει ότι θα έπρεπε να χάνει ενέργεια συνεχώς, εκπέμποντας ηλεκτρομαγνητικά κύματα. Καθώς η ενέργειά του μειώνεται, η τροχιά του θα σπειρώνεται προς τα μέσα, μέχρι να πέσει πάνω στον πυρήνα. Οι υπολογισμοί έδειξαν ότι αυτή η κατάρρευση θα γινόταν σε <10⁻¹¹ δευτερόλεπτα — λιγότερο από ένα εκατοστό του νανοδευτερολέπτου.
Σύμφωνα με τις εξισώσεις Maxwell, ένα ηλεκτρόνιο σε τροχιά γύρω από πρωτόνιο θα χάσει όλη του την ενέργεια σε περίπου 10⁻¹¹ δευτερόλεπτα. Κάθε άτομο στο Σύμπαν θα έπρεπε να έχει καταρρεύσει αμέσως μετά τη δημιουργία του. Η ύπαρξη σταθερής ύλης ήταν αδύνατη κλασικά — κάτι έπρεπε να αλλάξει ριζικά στην κατανόησή μας.
Η ύλη, όμως, υπάρχει. Τα άτομα είναι σταθερά, οι ηλεκτρονιακές δομές διατηρούνται, και η χημεία λειτουργεί. Αυτή η αντίφαση μεταξύ θεωρίας και πραγματικότητας ήταν μια από τις μεγαλύτερες κρίσεις στη φυσική των αρχών του 20ού αιώνα — και η λύση θα ερχόταν από έναν νεαρό Δανό φυσικό.
💡 Η Ιδέα του Μπορ (1913)
Ο Niels Bohr, γεννημένος στην Κοπεγχάγη το 1885, εργάστηκε στο εργαστήριο του Rutherford στο Μάντσεστερ, όπου αντιμετώπισε κατά πρόσωπο το πρόβλημα της ατομικής σταθερότητας. Τον Ιούλιο του 1913, δημοσίευσε μια σειρά τριών εργασιών με τίτλο «On the Constitution of Atoms and Molecules» που θα άλλαζαν τη φυσική για πάντα.
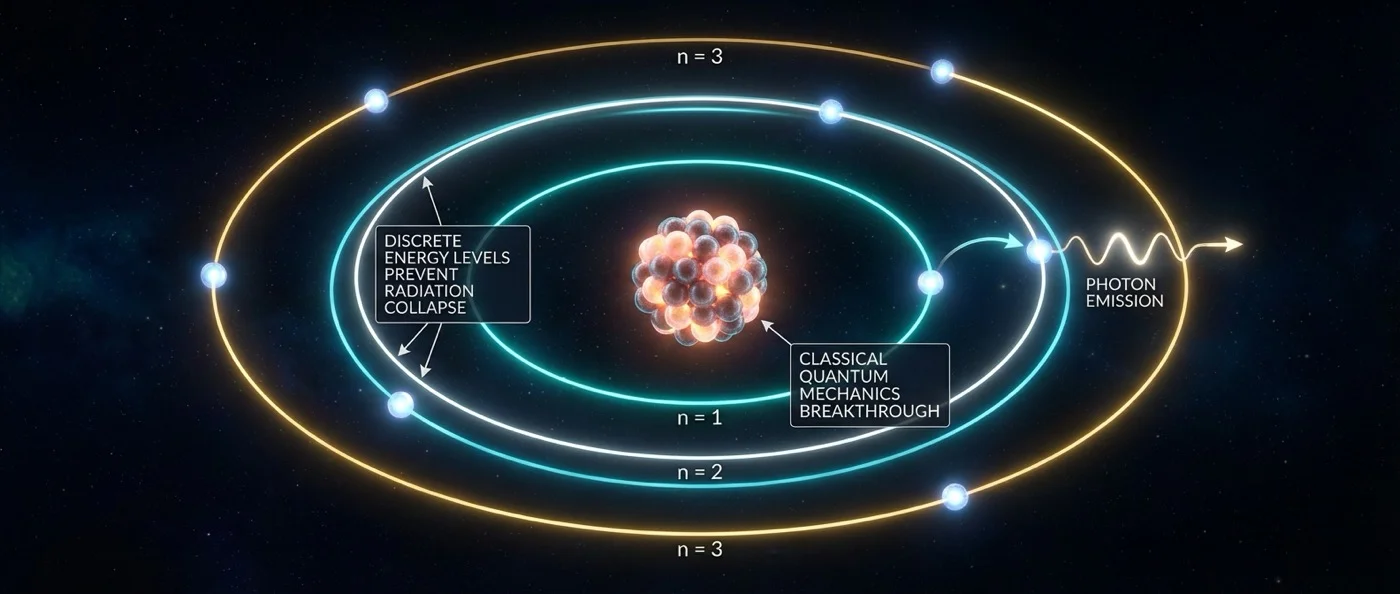
Ο Μπορ πρότεινε τρία τολμηρά αξιώματα. Πρώτον, τα ηλεκτρόνια μπορούν να κινούνται μόνο σε συγκεκριμένες τροχιές — τις λεγόμενες στάσιμες καταστάσεις. Δεύτερον, όταν βρίσκονται σε αυτές τις τροχιές, τα ηλεκτρόνια δεν εκπέμπουν ακτινοβολία, παρά τη συνεχή τους επιτάχυνση — μια ιδέα σε ευθεία αντίθεση με τη κλασική ηλεκτροδυναμική. Τρίτον, η ακτινοβολία εκπέμπεται ή απορροφάται μόνο όταν ένα ηλεκτρόνιο μεταπηδά (quantum jump) από μια επιτρεπτή τροχιά σε άλλη.
📖 Διαβάστε περισσότερα: Μαρί Κιουρί: Πώς η ραδιενέργεια άλλαξε την επιστήμη
Η βασική συνθήκη κβάντωσης του Μπορ ήταν ότι η στροφορμή του ηλεκτρονίου πρέπει να είναι ακέραιο πολλαπλάσιο της σταθεράς Planck: L = nℏ, όπου n = 1, 2, 3, ... και ℏ = h/2π. Αυτή η απλή αλλά επαναστατική ιδέα σήμαινε ότι δεν επιτρέπονται όλες οι τροχιές — μόνο εκείνες που ικανοποιούν τη συνθήκη κβάντωσης. Η ενέργεια δεν εκπέμπεται συνεχώς, αλλά σε διακριτά κβάντα.
Ο Μπορ ενσωμάτωσε έτσι τη σταθερά του Planck — που είχε εισαχθεί το 1900 για την ακτινοβολία μέλανος σώματος — απευθείας στη δομή του ατόμου. Η κβαντική ιδέα δεν αφορούσε πλέον μόνο το φως, αλλά και την ίδια την ύλη.
🌈 Εξήγηση του Φάσματος Υδρογόνου
Η μεγαλύτερη επιτυχία του μοντέλου Μπορ ήταν η εξήγηση του ατομικού φάσματος του υδρογόνου. Από τα τέλη του 19ου αιώνα, οι φυσικοί γνώριζαν ότι το υδρογόνο εκπέμπει φως σε πολύ συγκεκριμένα μήκη κύματος — διακριτές γραμμές στο φάσμα, αντί για μια συνεχή κατανομή. Ο Johann Balmer είχε ανακαλύψει ήδη το 1885 τον εμπειρικό τύπο που περιγράφει αυτές τις γραμμές στο ορατό φάσμα (σειρά Balmer), αλλά κανείς δεν μπορούσε να εξηγήσει γιατί υπάρχουν αυτές οι γραμμές.
Ο Μπορ απέδειξε ότι κάθε φασματική γραμμή αντιστοιχεί σε μεταπήδηση ηλεκτρονίου μεταξύ δύο ενεργειακών επιπέδων. Η ενέργεια του εκπεμπόμενου φωτονίου ισούται ακριβώς με τη διαφορά ενέργειας μεταξύ του αρχικού και του τελικού επιπέδου: E_φωτονίου = E_αρχικό − E_τελικό = hf, όπου f η συχνότητα του φωτός. Αυτός ο τύπος αναπαρήγαγε τέλεια τον τύπο Balmer και τον γενικευμένο τύπο Rydberg.
Η σειρά Balmer (μεταπηδήσεις προς n=2) αντιστοιχεί στο ορατό φάσμα. Η σειρά Lyman (προς n=1) δίνει υπεριώδη ακτινοβολία, ενώ οι σειρές Paschen, Brackett και Pfund (προς n=3, 4, 5 αντίστοιχα) εκπέμπουν υπέρυθρη. Όλες αυτές οι σειρές ακολουθούν ακριβώς τις προβλέψεις του μοντέλου Μπορ — μια ποσοτική επιτυχία που εντυπωσίασε τον επιστημονικό κόσμο.
📖 Διαβάστε περισσότερα: Ρίτσαρντ Φέυνμαν: Ο φυσικός που άλλαξε τον κόσμο
🔢 Ο Κβαντικός Αριθμός n
Στο μοντέλο Μπορ, κάθε επιτρεπτή τροχιά χαρακτηρίζεται από τον κύριο κβαντικό αριθμό n (n = 1, 2, 3, ...). Η ενέργεια κάθε επιπέδου δίνεται από τον τύπο:
E_n = −13.6 / n² eV
Η θεμελιώδης κατάσταση (ground state) αντιστοιχεί σε n=1, με ενέργεια −13.6 eV — αυτή είναι η ενέργεια ιονισμού του υδρογόνου, δηλαδή η ενέργεια που χρειάζεται για να αποσπαστεί πλήρως το ηλεκτρόνιο από τον πυρήνα. Οι διεγερμένες καταστάσεις (n=2, 3, 4, ...) έχουν υψηλότερη ενέργεια (λιγότερο αρνητική) και μεγαλύτερη ακτίνα τροχιάς.
Η ακτίνα τροχιάς αυξάνεται με n²: r_n = n² × 0.529 Å (ακτίνα Μπορ). Αυτό σημαίνει ότι η πρώτη τροχιά (n=1) έχει ακτίνα 0.529 Å, η δεύτερη (n=2) 2.116 Å, η τρίτη (n=3) 4.761 Å, και ούτω καθεξής. Η στροφορμή κβαντίζεται ως L = nℏ, δηλαδή μόνο ακέραια πολλαπλάσια της ανηγμένης σταθεράς Planck.
Καθώς n → ∞, η ενέργεια πλησιάζει το μηδέν και η ακτίνα τείνει στο άπειρο — το ηλεκτρόνιο «ξεφεύγει» και το άτομο ιονίζεται. Θεωρητικά υπάρχουν άπειρα ενεργειακά επίπεδα, αλλά πρακτικά τα πολύ υψηλά (Rydberg atoms) είναι εξαιρετικά ευαίσθητα σε εξωτερικές διαταραχές.
📖 Διαβάστε περισσότερα: Spin σωματιδίων: Η κβαντική ιδιότητα χωρίς ανάλογο
🔬 Περιορισμοί του Μοντέλου
Παρά τη θριαμβευτική εξήγηση του φάσματος υδρογόνου, το μοντέλο Μπορ είχε σημαντικούς περιορισμούς. Ο πρώτος και πιο προφανής ήταν ότι λειτουργούσε μόνο για υδρογονοειδή άτομα — δηλαδή άτομα με ένα μόνο ηλεκτρόνιο (υδρογόνο, He⁺, Li²⁺). Για τα πολυηλεκτρονιακά άτομα, το μοντέλο αποτύγχανε εντελώς, επειδή δεν μπορούσε να αντιμετωπίσει τις αλληλεπιδράσεις μεταξύ ηλεκτρονίων.
Δεύτερον, το μοντέλο δεν εξηγούσε τη λεπτή δομή (fine structure) των φασματικών γραμμών — τη διάσπαση κάθε γραμμής σε πολύ κοντινές γραμμές, η οποία εξαρτάται από σχετικιστικές διορθώσεις και τη σύζευξη τροχιακής-spin στροφορμής. Ούτε μπορούσε να εξηγήσει το φαινόμενο Zeeman — τη διάσπαση φασματικών γραμμών παρουσία μαγνητικού πεδίου.
Τρίτον, το μοντέλο αντιμετώπιζε το ηλεκτρόνιο ως σωματίδιο σε καθορισμένη τροχιά, αγνοώντας την κυματική φύση του — κάτι που θα αποδεικνυόταν θεμελιώδες μέσα στην επόμενη δεκαετία. Ο Μπορ είχε κάνει ένα σωστό βήμα, αλλά η κατανόηση της πλήρους εικόνας απαιτούσε ριζικά νέα εργαλεία.
«Αν η κβαντική μηχανική δεν σε έχει σοκάρει βαθιά, σημαίνει ότι δεν την έχεις κατανοήσει ακόμα.» — Niels Bohr
🚀 Από τον Μπορ στην Κβαντομηχανική
Το μοντέλο Μπορ, παρά τους περιορισμούς του, άνοιξε τον δρόμο για την πλήρη κβαντική θεωρία. Το 1924, ο Louis de Broglie πρότεινε ότι τα ηλεκτρόνια — και γενικά όλα τα σωματίδια — έχουν κυματικές ιδιότητες. Το μήκος κύματος de Broglie δίνεται από τη σχέση λ = h/p, όπου p η ορμή. Αυτή η ιδέα εξηγούσε αμέσως τη συνθήκη κβάντωσης του Μπορ: οι επιτρεπτές τροχιές αντιστοιχούν ακριβώς σε εκείνες στις οποίες χωράει ακέραιος αριθμός μηκών κύματος — στάσιμα κύματα γύρω από τον πυρήνα.
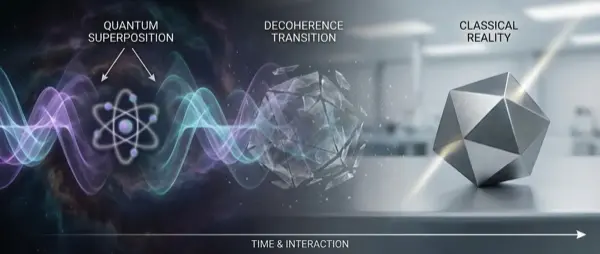
Το 1926, ο Erwin Schrödinger διατύπωσε τη δική του εκδοχή της κβαντικής μηχανικής βασισμένη στην εξίσωση κύματος. Η εξίσωση Schrödinger περιγράφει το ηλεκτρόνιο όχι ως σημειακό σωματίδιο σε τροχιά, αλλά ως κυματοσυνάρτηση ψ(r) κατανεμημένη στον χώρο. Το |ψ|² δίνει την πιθανότητα εύρεσης του ηλεκτρονίου σε δεδομένη θέση — η κλασική τροχιά αντικαταστάθηκε από ένα νέφος πιθανότητας.
Η μετάβαση από τροχιές (orbits) σε τροχιακά (orbitals) ήταν εννοιολογική επανάσταση. Στη σύγχρονη κβαντική μηχανική, ένα τροχιακό δεν είναι ένα μονοπάτι αλλά μια τρισδιάστατη περιοχή χώρου με χαρακτηριστικό σχήμα (s, p, d, f) και ενέργεια. Το ηλεκτρόνιο δεν «κυκλοφορεί» σε συγκεκριμένο δρόμο — υπάρχει ως κύμα πιθανότητας μέχρι τη στιγμή της μέτρησης.
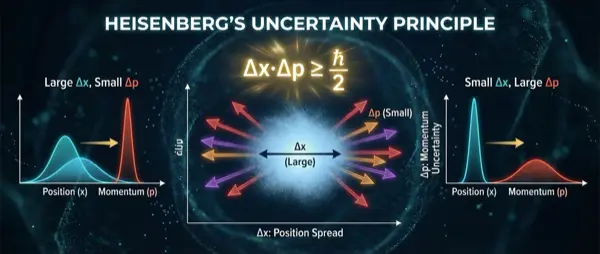
Παράλληλα, ο Werner Heisenberg ανέπτυξε τη μηχανική πινάκων (1925), που αποδείχτηκε μαθηματικά ισοδύναμη με την κυματομηχανική του Schrödinger. Η αρχή της απροσδιοριστίας του Heisenberg (Δx · Δp ≥ ℏ/2) σφράγισε τη μετάβαση: δεν μπορούμε ποτέ να γνωρίζουμε ταυτόχρονα με ακρίβεια τη θέση και την ορμή ενός ηλεκτρονίου — η ίδια η έννοια της «τροχιάς» χάνει νόημα σε κβαντικό επίπεδο.
Το μοντέλο Μπορ αποτελεί σήμερα μια ιστορική γέφυρα: η πρώτη επιτυχημένη σύνθεση κλασικής φυσικής και κβαντικών ιδεών, που μας οδήγησε στο πλαίσιο κατανόησης που χρησιμοποιούμε μέχρι σήμερα. Από τον Πλανκ στον Μπορ, και από τον Μπορ στον Σρέντινγκερ, κάθε βήμα αποκάλυπτε ότι η φύση, στη μικρότερη κλίμακα, δεν λειτουργεί με τους κανόνες του «μεγάλου κόσμου» — αλλά με τους δικούς της, βαθύτερους νόμους.