📖 Διαβάστε ακόμα: Τεστ Αίματος Βλέπει το Alzheimer 4 Χρόνια Πριν Εμφανιστεί
🔬 Η Ανακάλυψη του Ενζύμου CaMKK2
Μια ομάδα ερευνητών από το Πανεπιστήμιο Monash της Μελβούρνης και το Baylor College of Medicine του Τέξας δημοσίευσε μελέτη-ορόσημο στο επιστημονικό περιοδικό Molecular Metabolism, αναδεικνύοντας τον ρόλο-κλειδί ενός ενζύμου με την ονομασία CaMKK2 (calcium/calmodulin-dependent protein kinase kinase 2). Πρόκειται για ένα μόριο που λειτουργεί ως κεντρικός ρυθμιστής του ενεργειακού μεταβολισμού σε ολόκληρο το σώμα, συντονίζοντας παράλληλα τις φλεγμονώδεις αποκρίσεις των μακροφάγων — ανοσοκυττάρων που βρίσκονται στους ιστούς μας και είναι υπεύθυνα για την «κατάποση» βακτηρίων, κατεστραμμένων κυττάρων και εισβολέων.
Όπως εξηγεί ο Dr. John Scott, ανώτερος ερευνητής του Monash Institute of Pharmaceutical Sciences: «Η παχυσαρκία συνδέεται με μια συνεχή, χαμηλού βαθμού φλεγμονή σε βασικά όργανα που ελέγχουν τον μεταβολισμό, όπως το ήπαρ, ο λιπώδης ιστός και οι μύες. Αυτή η φλεγμονή παίζει ρόλο σε παθήσεις όπως η αντίσταση στην ινσουλίνη και ο διαβήτης τύπου 2.» Ο βασικός μοχλός αυτής της διαδικασίας είναι η συσσώρευση μακροφάγων στα όργανα αυτά: όταν το σώμα βρίσκεται υπό πίεση — π.χ. από μια δίαιτα υψηλή σε λιπαρά — τα φλεγμονώδη μακροφάγα στρέφονται σε ταχύτερους αλλά λιγότερο αποδοτικούς τρόπους παραγωγής ενέργειας.
🧪 Το Πείραμα: Ποντίκια Χωρίς CaMKK2
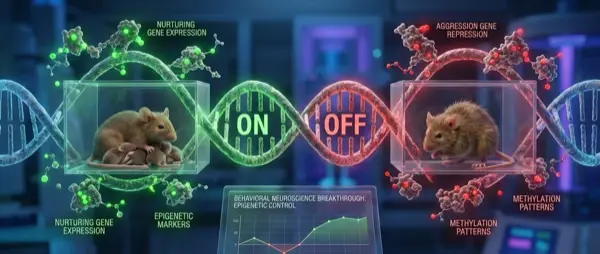
Οι επιστήμονες δημιούργησαν γενετικά τροποποιημένα ποντίκια στα οποία το ένζυμο CaMKK2 είχε αφαιρεθεί αποκλειστικά από τα μυελοειδή κύτταρα — μια ομάδα ανοσοκυττάρων που περιλαμβάνει μακροφάγα, ουδετερόφιλα και δενδριτικά κύτταρα. Τα τροποποιημένα ποντίκια, μαζί με κανονικά ποντίκια ελέγχου, τράφηκαν με δίαιτα υψηλή σε λιπαρά για αρκετές εβδομάδες.
Τα αποτελέσματα ήταν εντυπωσιακά. Ενώ τα κανονικά ποντίκια πάχυναν σημαντικά, τα ποντίκια χωρίς CaMKK2 αντιστάθηκαν πλήρως στην αύξηση βάρους και λιπώδους μάζας — παρόλο που έτρωγαν την ίδια ποσότητα τροφής. Ο λόγος; Τα τροποποιημένα ζώα έκαιγαν περισσότερη ενέργεια. Παρουσίασαν επίσης χαμηλότερα επίπεδα σακχάρου αίματος, βελτιωμένη ανοχή γλυκόζης, καλύτερη ευαισθησία στην ινσουλίνη, και πλήρη προστασία από τη λιπώδη νόσο του ήπατος.
⚙️ Πώς Λειτουργεί ο Διακόπτης
Σε φυσιολογική παχυσαρκία, τα μακροφάγα στον λιπώδη ιστό μεταπίπτουν σε μια φλεγμονώδη κατάσταση, η οποία οδηγεί σε αντίσταση στην ινσουλίνη. Χωρίς το CaMKK2, οι ερευνητές ανακάλυψαν ότι αυτή η αλυσίδα αντιδράσεων αναστρέφεται ριζικά. Τα μακροφάγα χωρίς το ένζυμο είχαν ένα αντιφλεγμονώδες προφίλ, παρήγαγαν ελάχιστα φλεγμονώδη σήματα, και έδειχναν εμφανή προτίμηση στην καύση λίπους ως καύσιμο μέσω αυξημένης οξείδωσης λιπαρών οξέων.
Παράλληλα, η μιτοχονδριακή λειτουργία των κυττάρων αυτών βελτιώθηκε δραματικά — τα μιτοχόνδρια, τα «εργοστάσια ενέργειας» του κυττάρου, δούλευαν πιο αποτελεσματικά. Το αποτέλεσμα δεν περιορίστηκε στα ανοσοκύτταρα: ολόκληρος ο λιπώδης ιστός αναδιαμορφώθηκε. Εμφάνισε φαινόμενο «μπεζ μετατροπής» (beiging), κατά το οποίο γονιδιακά προγράμματα που προωθούν την καύση λίπους και τη θερμογένεση ενεργοποιήθηκαν.
🔑 Γιατί Είναι Σημαντική Αυτή η Ανακάλυψη
Σε αντίθεση με τα φάρμακα GLP-1 (όπως το Ozempic) που μειώνουν κυρίως την όρεξη, η στόχευση του CaMKK2 δρα σε εντελώς διαφορετικό επίπεδο: αναπρογραμματίζει τον τρόπο που τα ανοσοκύτταρα διαχειρίζονται την ενέργεια. Τα ποντίκια δεν έτρωγαν λιγότερο — έκαιγαν περισσότερα. Αυτό σημαίνει ότι θα μπορούσε να αναπτυχθεί συνδυαστική θεραπεία, χτυπώντας την παχυσαρκία ταυτόχρονα από δύο μέτωπα: μείωση πρόσληψης τροφής και αύξηση ενεργειακής δαπάνης.
📖 Διαβάστε ακόμα: Βλαστοκύτταρο Παράγει 14 Εκατ. NK Κύτταρα κατά Καρκίνου
🧬 Από Λευκό σε Μπεζ: Η Μαγεία της Θερμογένεσης
Για να κατανοήσουμε πλήρως τη σημασία αυτής της ανακάλυψης, χρειάζεται μια σύντομη εξήγηση για τα είδη λιπώδους ιστού. Το σώμα μας περιέχει τρεις βασικούς τύπους λίπους: το λευκό, που αποθηκεύει ενέργεια· το φαιό (brown fat), που καίει ενέργεια παράγοντας θερμότητα· και το μπεζ, που βρίσκεται κάπου στη μέση — ξεκινά ως λευκό αλλά μπορεί να «ενεργοποιηθεί» για να καίει ενέργεια όπως το φαιό.
Η μετατροπή λευκών λιποκυττάρων σε μπεζ — η λεγόμενη «μπεζ μεταμόρφωση» — αποτελεί έναν από τους πιο ελκυστικούς θεραπευτικούς στόχους στην έρευνα κατά της παχυσαρκίας. Αντί να αφαιρέσεις λίπος, το αναγκάζεις να καεί εσωτερικά. Η μελέτη για το CaMKK2 έδειξε ότι η απενεργοποίηση του ενζύμου σε μακροφάγα ενεργοποιεί ακριβώς αυτή τη διαδικασία στον λιπώδη ιστό.
Η ανακάλυψη αυτή δεν είναι μεμονωμένη. Μια ιστορική μελέτη του MIT και της Harvard Medical School, δημοσιευμένη στο New England Journal of Medicine, αποκάλυψε νωρίτερα τον αντίστοιχο γενετικό μηχανισμό: στη γονιδιωματική περιοχή FTO, μια αλλαγή ενός μόνο νουκλεοτιδίου καθορίζει αν τα γονίδια IRX3 και IRX5 θα ενεργοποιηθούν, κλείνοντας τη θερμογένεση και οδηγώντας σε συσσώρευση λίπους. Με τη χρήση CRISPR/Cas9 οι ερευνητές μπόρεσαν να εναλλάσσουν μεταξύ «αδύνατου» και «παχύσαρκου» μεταβολικού προφίλ σε ανθρώπινα κύτταρα.
«Τα ευρήματά μας δείχνουν ότι όταν αφαιρεθεί το γονίδιο CaMKK2 από ορισμένα ανοσοκύτταρα, ο λιπώδης ιστός αλλάζει τη δραστηριότητά του προς μια υγιέστερη κατεύθυνση. Τα γονίδια στο λίπος αρχίζουν να λειτουργούν με τρόπους που υποστηρίζουν καλύτερο μεταβολισμό και μειώνουν την επιβλαβή φλεγμονή.»
🏥 Η Ευρύτερη Εικόνα: Νέα Μέτωπα Κατά της Παχυσαρκίας
Η ανακάλυψη για το CaMKK2 εντάσσεται σε ένα ρεύμα πρόσφατων ερευνών που αλλάζουν ριζικά την κατανόηση της παχυσαρκίας ως νόσου. Τον Ιανουάριο 2026, ερευνητές του KAIST στη Νότια Κορέα ταυτοποίησαν έναν επιγενετικό διακόπτη μέσω των πρωτεϊνών YAP και TAZ, οι οποίες μπορούν να μπλοκάρουν τη δημιουργία νέων λιποκυττάρων αναστέλλοντας τον «αρχιρυθμιστή» PPARγ. Σε ποντίκια, η απενεργοποίηση του συστήματος Hippo που ρυθμίζει τις YAP/TAZ οδήγησε σε αναστροφή της ωρίμανσης λιποκυττάρων — τα κύτταρα «ξεμαθαίνουν» πώς να είναι λιποκύτταρα.
Παράλληλα, τον Δεκέμβριο 2025, ερευνητές στη Βραζιλία ανακάλυψαν ότι η ορμόνη FGF19 — που παράγεται κυρίως στο λεπτό έντερο — στέλνει σήματα στον υποθάλαμο του εγκεφάλου, ενεργοποιώντας θερμογενετικά λιποκύτταρα μέσω του συμπαθητικού νευρικού συστήματος. Η FGF19 όχι μόνο αυξάνει την ενεργειακή δαπάνη αλλά μειώνει και τη φλεγμονή στους περιφερικούς ιστούς. Η προσέγγιση αυτή μοιάζει με τον μηχανισμό δράσης του σεμαγλουτιδίου (Ozempic), αλλά λειτουργεί μέσω εντελώς διαφορετικών υποδοχέων.
Κάθε μία από αυτές τις ανακαλύψεις προσφέρει ένα διαφορετικό «κουμπί» στον πίνακα ελέγχου του μεταβολισμού. Η στόχευση του CaMKK2 αλλάζει τη συμπεριφορά των ανοσοκυττάρων. Η YAP/TAZ επηρεάζει τη δημιουργία λιποκυττάρων. Η FGF19 ενεργοποιεί εγκεφαλικά μονοπάτια θερμογένεσης. Μαζί, σκιαγραφούν μια πολυεπίπεδη στρατηγική κατά της παχυσαρκίας που θα μπορούσε να αντικαταστήσει — ή να συμπληρώσει — τα σημερινά φάρμακα.
⚠️ Προκλήσεις και Επόμενα Βήματα
Παρά τον ενθουσιασμό, υπάρχουν σημαντικοί περιορισμοί. Τα ευρήματα προέρχονται κυρίως από ζωικά μοντέλα και δεν έχουν εφαρμοστεί ακόμη σε ανθρώπους. Η ένωση STO-609, που χρησιμοποιείται για την αναστολή του CaMKK2, δεν είναι αρκετά εκλεκτική και έχει κακές φαρμακοκινητικές ιδιότητες, καθιστώντας την ακατάλληλη για κλινική χρήση. Χρειάζεται ανάπτυξη νέων, εκλεκτικών αναστολέων με φαρμακευτικό δυναμικό.
Επιπλέον, ενώ τα μακροφάγα εμφάνισαν αυξημένη καύση λιπαρών οξέων σε εργαστηριακά πιάτα, δεν αποδείχθηκε άμεσα ότι αυτό συμβαίνει στον ίσο βαθμό μέσα σε ζωντανούς οργανισμούς. Ωστόσο, η ερευνητική ομάδα είναι αισιόδοξη: δεδομένου ότι η φλεγμονή που οδηγείται από μακροφάγα εμπλέκεται επίσης στην αθηροσκλήρωση, σε λοιμώξεις και σε ορισμένους καρκίνους, η αναστολή του CaMKK2 θα μπορούσε να έχει πολύ ευρύτερα οφέλη.
Η παχυσαρκία δεν είναι πλέον μια απλή εξίσωση «θερμίδες μέσα, θερμίδες έξω». Οι ανακαλύψεις αυτές δείχνουν ότι κρυφοί μοριακοί διακόπτες καθορίζουν αν το σώμα μας θα αποθηκεύσει ή θα κάψει ενέργεια — και ότι η επιστήμη βρίσκεται πιο κοντά από ποτέ στο να τους χειριστεί. Αν οι εργαστηριακές υποσχέσεις μεταφραστούν σε θεραπείες, η επόμενη γενιά φαρμάκων κατά της παχυσαρκίας μπορεί να μη μας ζητά απλώς να τρώμε λιγότερο — αλλά να «αναπρογραμματίζει» τον τρόπο που ο οργανισμός μας επεξεργάζεται το λίπος.
📚 Πηγές
- • Scott, J. et al. (2025). CaMKK2 in myeloid cells and diet-induced obesity. Molecular Metabolism. Monash University / Baylor College of Medicine.
- • Claussnitzer, M. et al. (2015). FTO Obesity Variant Circuitry and Adipocyte Browning in Humans. New England Journal of Medicine. MIT / Harvard.
- • Lim, D.S. et al. (2026). Epigenetic control of adipocyte differentiation via Hippo-YAP/TAZ. Science Advances. KAIST.
- • Zangerolamo, L. et al. (2025). Central FGF19 signaling and adipose tissue thermogenesis. American Journal of Physiology. UNICAMP / Harvard.