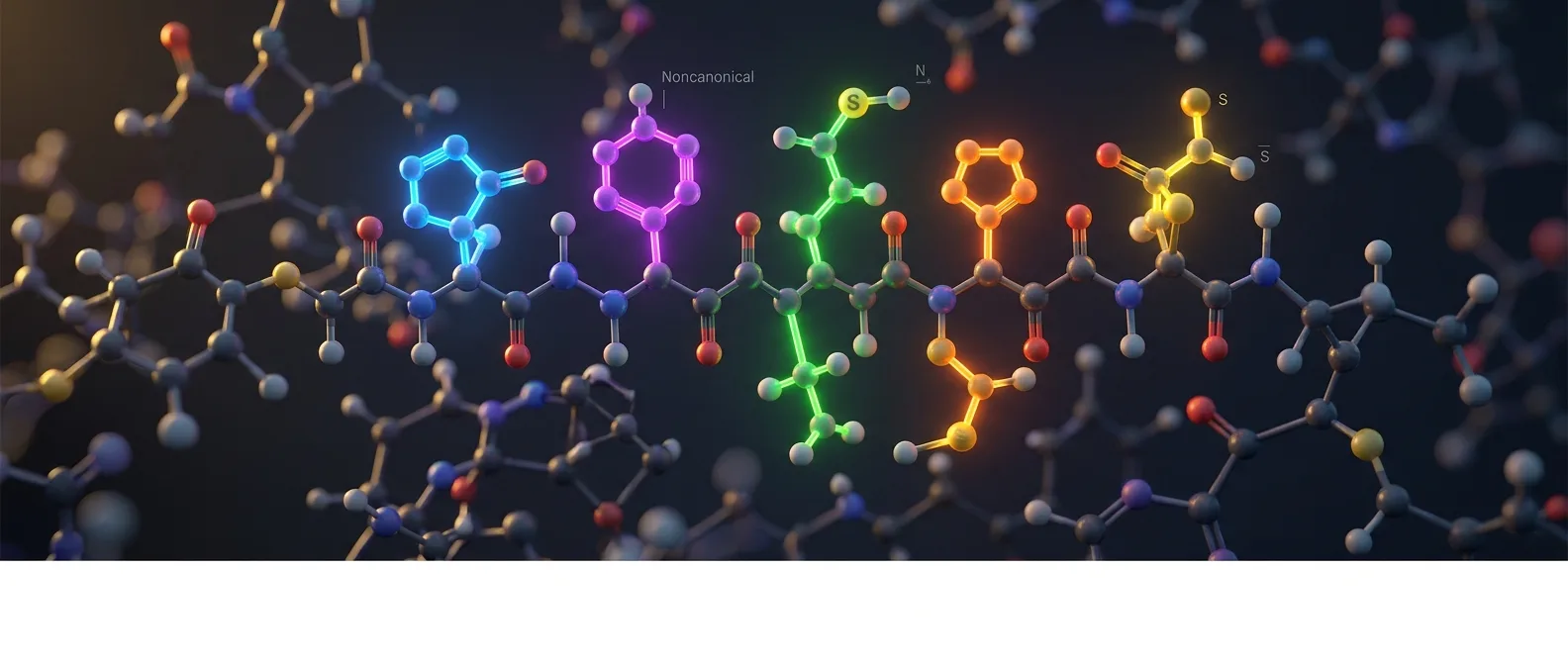
Έξι σημεία ενσωμάτωσης μη κανονικών αμινοξέων σε έναν πρωτεΐνη — αυτό είναι το νέο ρεκόρ που κατέκτησαν ερευνητές του 2026. Πίσω από αυτή την επιτυχία κρύβεται μια τελείως διαφορετική προσέγγιση στη γενετική μηχανική που αφήνει πίσω τις παραδοσιακές μεθόδους και στρέφεται στους λεγόμενους σπάνιους κωδικώνες (rare codons).
Οι παραδοσιακές τεχνικές επέκτασης του γενετικού κώδικα είχαν σαφή όρια. Όταν οι ερευνητές ήθελαν να εντάξουν μη κανονικά αμινοξέα σε πρωτεΐνες, έπρεπε να χρησιμοποιήσουν stop codons — τα σήματα που λένε στο κύτταρο να σταματήσει την παραγωγή πρωτεΐνης. Η μέθοδος λειτουργούσε, αλλά με χαμηλή απόδοση και περιορισμένες δυνατότητες.
📖 Διαβάστε ακόμα: 10 Ζώα που Λάμπουν στο Σκοτάδι: Βιοφωταύγεια στη Φύση
🔬 Το Μυστικό των Σπάνιων Κωδικώνων
Η νέα τεχνική που αναπτύχθηκε το 2024 και βελτιώθηκε φέτος δεν χρησιμοποιεί stop codons, αλλά εκμεταλλεύεται κάτι πολύ πιο έξυπνο. Οι ερευνητές ανακάλυψαν ότι κάποιοι κωδικώνες — συγκεκριμένα ο TCG — είναι τόσο σπάνιοι στα μαμμαλιακά κύτταρα που μπορούν να τους "κλέψουν" χωρίς να επηρεαστεί η φυσιολογική λειτουργία.
Φανταστείτε το σαν μια παλιά πόλη όπου κάποιοι δρόμοι χρησιμοποιούνται τόσο λίγο που μπορείτε να τους κατεδαφίσετε και να φτιάξετε κάτι νέο χωρίς να επηρεάσετε την κίνηση. Ο κωδικώνας TCG, που κανονικά κωδικοποιεί τη σερίνη, εμφανίζεται τόσο σπάνια που η αντικατάστασή του δεν δημιουργεί προβλήματα.
Η Στατιστική Πίσω από την Επανακωδικοποίηση
Σε έναν τυπικό αυτοσωματικό χρωμοσώμα ποντικού, ο κωδικώνας TCG εμφανίζεται μόλις 46.635 φορές, σε σύγκριση με τον κωδικώνα TTC που εμφανίζεται 473.915 φορές. Αυτή η 10πλάσια διαφορά επιτρέπει την ασφαλή επανακωδικοποίηση.
⚡ Πέντε Διαφορετικά Αμινοξέα Ταυτόχρονα
Αυτό που καθιστά την ανακάλυψη πραγματικά επαναστατική δεν είναι μόνο η νέα τεχνική, αλλά και οι δυνατότητές της. Χρησιμοποιώντας συνδυασμό σπάνιων κωδικώνων και βελτιωμένων stop codons, οι ερευνητές κατάφεραν να ενσωματώσουν πέντε εντελώς διαφορετικά μη κανονικά αμινοξέα στην ίδια πρωτεΐνη.
Μιλάμε για πρωτεΐνες με φθοριζόντα αμινοξέα για ανίχνευση, με κλικ-χημεία για βιοσύνδεση, ή ακόμα και με φωτο-ενεργοποιήσιμες ομάδες που αλλάζουν τη συμπεριφορά της πρωτεΐνης μόνο όταν δεχτούν φως συγκεκριμένης συχνότητας. Δηλαδή, από την απλή παρατήρηση πρωτεϊνών μέχρι τον ακριβή έλεγχο της δραστικότητάς τους.
Τα Νέα Αμινοξέα και οι Ιδιότητές τους
Κάθε μη κανονικό αμινοξέα φέρνει τη δική του "υπερδύναμη". Ένα από τα πιο ενδιαφέροντα είναι το trans-cyclooct-2-en-1-yl αμινοξύ που επιτρέπει βιοορθογώνιες αντιδράσεις — δηλαδή χημικές αντιδράσεις που λειτουργούν μόνο εντός του βιολογικού περιβάλλοντος χωρίς να επηρεάζουν άλλες διεργασίες.
Ένα άλλο είναι το azido-phenylalanine που λειτουργεί σαν χημικό αγκίστρι. Μπορεί να συνδεθεί με οποιοδήποτε μόριο έχει την κατάλληλη "κλειδαριά", επιτρέποντας την προσάρτηση φαρμάκων, σημαντικών μορίων ή ακόμα και άλλων πρωτεϊνών σε ακριβώς καθορισμένα σημεία.
📖 Διαβάστε ακόμα: 18.000 Ίχνη Δεινοσαύρων σε Βράχο της Βολιβίας
🧬 Η Μηχανική Πίσω από την Επιτυχία
Το κλειδί της τεχνικής βρίσκεται στη συστηματική μηχανική τριών κρίσιμων στοιχείων. Πρώτον, οι ερευνητές ανέπτυξαν ορθογώνια ζεύγη αμινοακυλο-tRNA συνθετάσης και tRNA που αναγνωρίζουν αποκλειστικά τους επανακωδικοποιημένους κωδικώνες. Δεύτερον, βελτιστοποίησαν το μηχανισμό μεταφοράς των μη κανονικών αμινοξέων στο κύτταρο. Τρίτον, χρησιμοποίησαν μοντέλα τεχνητής νοημοσύνης για να προβλέψουν ποιοι κωδικώνες θα λειτουργούσαν καλύτερα.
Η χρήση AI στη γενετική μηχανική είναι σχετικά νέα, αλλά εδώ απέδωσε εντυπωσιακά. Αντί οι ερευνητές να δοκιμάζουν τυφλά διαφορετικούς συνδυασμούς κωδικώνων και αμινοξέων, τα αλγόριθμα προέβλεπαν ποιες παραλλαγές θα είχαν την υψηλότερη απόδοση.
📖 Διαβάστε ακόμα: Δεν Έχουμε 5 Αισθήσεις αλλά 33: Ποιες οι Κρυμμένες;
🔧 Πρακτικές Εφαρμογές στη Βιοτεχνολογία
Πέρα από τις εντυπωσιακές δυνατότητες, η τεχνική έχει άμεσες πρακτικές εφαρμογές. Στη φαρμακευτική βιομηχανία, επιτρέπει τη δημιουργία πρωτεϊνών με βελτιωμένη σταθερότητα και εκλεκτικότητα. Στην ιατρική, ανοίγει το δρόμο για πιο αποτελεσματικές θεραπείες γονιδίων και καλύτερα διαγνωστικά εργαλεία.
Ένα συγκεκριμένο παράδειγμα αφορά τη δημιουργία μακροκυκλικών πεπτιδίων — μορίων που συμπεριφέρονται σαν φάρμακα αλλά έχουν πολύ μεγαλύτερη αντοχή και εκλεκτικότητα. Με τη νέα τεχνική, αυτά τα πεπτίδια μπορούν να παραχθούν απευθείας μέσα σε βιολογικά συστήματα, μειώνοντας δραστικά το κόστος παραγωγής.
Μοριακή Ρολογοποιία στον Χρόνο
Μια από τις πιο συναρπαστικές εφαρμογές είναι η δημιουργία "χρονοκαθοδηγούμενων" πρωτεϊνών. Ενσωματώνοντας φωτο-αποικοδομήσιμα αμινοξέα σε κρίσιμα σημεία, οι ερευνητές μπορούν να ελέγχουν πότε ακριβώς μια πρωτεΐνη θα ενεργοποιηθεί ή θα απενεργοποιηθεί. Απλά με την έκθεση σε φως συγκεκριμένου μήκους κύματος.
Αυτό σημαίνει θεραπείες που ενεργοποιούνται μόνο στον στόχο τους, διαγνωστικά που "ανάβουν" μόνο παρουσία της ασθένειας, ή βιοκαταλύτες που λειτουργούν μόνο όταν τους χρειαζόμαστε. Είναι σαν να έχουμε διακόπτη on/off για τις βιολογικές διεργασίες.
💡 Προκλήσεις και Περιορισμοί
Βέβαια, η τεχνική δεν είναι χωρίς προκλήσεις. Η επανακωδικοποίηση σπάνιων κωδικώνων απαιτεί εκτεταμένη επαλήθευση ότι δεν επηρεάζει άλλες πρωτεΐνες του κυττάρου. Επίσης, κάθε νέο μη κανονικό αμινοξύ πρέπει να περάσει μέσα από την κυτταρική μεμβράνη — κάτι που δεν είναι πάντα εύκολο.
Ένα σημαντικό πρακτικό εμπόδιο παραμένει το κόστος των μη κανονικών αμινοξέων. Παρότι η νέα τεχνική αυξάνει την απόδοση, πολλά από αυτά τα εξειδικευμένα μόρια είναι ακόμα ακριβά για βιομηχανική χρήση. Μάλλον θα χρειαστούν νέες βιοσυνθετικές οδοί για την παραγωγή τους.
"Δεν αρκεί να μπορούμε να το κάνουμε — πρέπει να το κάνουμε αποδοτικά και οικονομικά. Αυτό είναι το επόμενο μεγάλο εμπόδιο για την ευρεία εφαρμογή της τεχνολογίας."
Ερευνητής στη συνθετική βιολογία
📖 Διαβάστε ακόμα: Αλεπού Αρπάζει Λυκόπουλο: Πρώτη Φορά σε Κάμερα
📊 Συγκριτική Ανάλυση με Προηγούμενες Μεθόδους
Το πλεονέκτημα της νέας προσέγγισης γίνεται ξεκάθαρο όταν τη συγκρίνουμε με τις παραδοσιακές τεχνικές. Οι μέθοδοι που βασίζονται σε amber stop codons επιτυγχάνουν συνήθως 10-30% απόδοση ενσωμάτωσης μη κανονικών αμινοξέων. Η επανακωδικοποίηση σπάνιων κωδικώνων φτάνει το 80-95%.
Αλλά η πραγματική διαφορά δεν είναι μόνο στους αριθμούς. Η παλιά τεχνική περιοριζόταν σε ένα, το πολύ δύο μη κανονικά αμινοξέα ανά πρωτεΐνη. Η νέα επιτρέπει πέντε ή έξι διαφορετικά, δίνοντας εντελώς νέες δυνατότητες στη μοριακή σχεδίαση.
Τι Σημαίνει για τους Ερευνητές
Για τους ερευνητές που δουλεύουν με πρωτεΐνες, η αλλαγή είναι σημαντική. Αντί να σχεδιάζουν γύρω από τους περιορισμούς της τεχνολογίας, μπορούν τώρα να εστιάσουν στη βιολογική λειτουργία που θέλουν να επιτύχουν. Είναι η διαφορά μεταξύ του να ζωγραφίζεις με τρία χρώματα ή με όλη την παλέτα.
Ιδιαίτερα στη δομική βιολογία και την ενζυμολογία, όπου η ακριβής τοποθέτηση φθοριζόντων ή άλλων λειτουργικών ομάδων είναι κρίσιμη, η δυνατότητα πολλαπλών τροποποιήσεων ανά πρωτεΐνη αλλάζει θεμελιωδώς τις δυνατότητες πειραματισμού.
🔮 Μελλοντικές Κατευθύνσεις
Η τρέχουσα έρευνα εστιάζει στη διεύρυνση του φάσματος των διαθέσιμων μη κανονικών αμινοξέων και στη βελτιστοποίηση των βιοσυνθετικών οδών για την οικονομική τους παραγωγή. Στόχος είναι να φτάσουμε σε σημείο όπου η επανακωδικοποίηση να είναι τόσο εύκολη όσο το cloning.
Παράλληλα, αναπτύσσονται νέα εργαλεία που θα επιτρέψουν την πρόβλεψη και το σχεδιασμό βελτιωμένων πρωτεϊνών με τεχνητή νοημοσύνη. Αν η πρόβλεψη πτυχώσεων με AlphaFold ήταν το πρώτο κύμα, η σχεδίαση πρωτεϊνών με μη κανονικά αμινοξέα είναι το επόμενο.
Μακροπρόθεσμα, η τεχνολογία μπορεί να οδηγήσει σε εντελώς νέες κατηγορίες βιοϋλικών και θεραπευτικών. Πρωτεΐνες που αυτο-επισκευάζονται, ένζυμα που λειτουργούν σε ακραίες συνθήκες, ή ακόμα και βιολογικά συστήματα που μπορούν να "προγραμματιστούν" για συγκεκριμένες εργασίες.
Ωστόσο, όπως συμβαίνει συχνά με πρωτοποριακές τεχνολογίες, η απόσταση από το εργαστήριο στην κλινική ή τη βιομηχανία είναι μεγάλη. Πόσο γρήγορα θα τη διανύσουμε εξαρτάται όσο από την τεχνική πρόοδο, άλλο τόσο και από την οικονομική βιωσιμότητα των εφαρμογών. Και εκεί ακόμα περιμένουμε απαντήσεις.